Cục Quản lý Dược cho biết đã nhận được văn bản ngày 22/12 và hồ sơ, tài liệu kèm theo của Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam về đề nghị tiêm liều thứ 3 của vắc xin Spikevax (vắc xin Covid-19 Moderna)
Căn cứ kết luận của Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc ngày 9/1, Cục Quản lý Dược đồng ý với đề nghị tiêm liều tăng cường (liều thứ ba) của vắc xin Spikevax (tên khác là vắc xin Moderna) theo hướng dẫn của cơ sở sản xuất vắc xin.
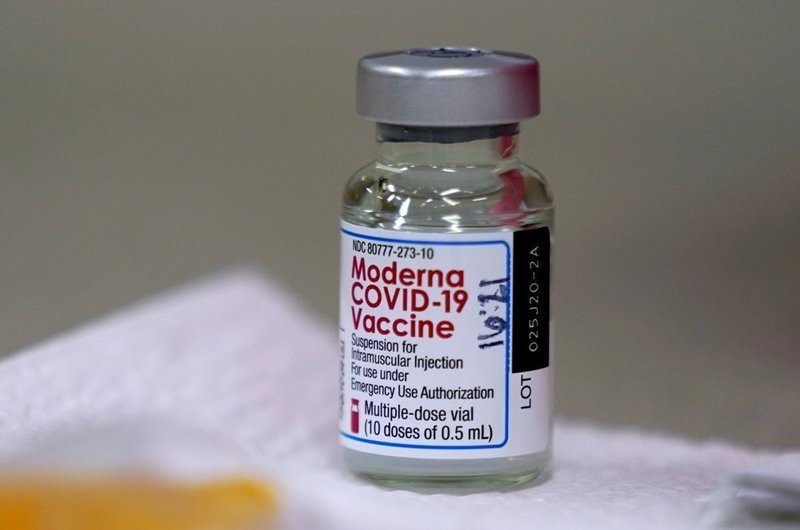
| Mũi vắc xin Covid-19 thứ 3 của Moderna sẽ bằng nửa liều cơ bản |
Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam phải hoàn toàn chịu trách nhiệm trước pháp luật về chất lượng, an toàn đối với vắc xin Spikevax (vắc xin Moderna) lưu hành trên thị trường. Đồng thời, có trách nhiệm thông báo ngay sự thay đổi này đến Cục Quản lý Dược và các đơn vị có liên quan.
Theo hướng dẫn của nhà sản xuất vắc xin Spikevax (vắc xin Moderna), đối với liều cơ bản cho người từ 12 tuổi trở lên, vắc xin này được sử dụng theo liệu trình gồm 2 liều 100mcg (mỗi liều 0,5ml), khuyến cáo tiêm liều thứ hai vào 28 ngày sau liều đầu tiên.
Đối với liều thứ 3 cho người từ 18 tuổi trở lên, một liều bổ sung (0,25ml, chứa 50mcg mNRA, bằng một nửa liều cơ bản) của Spikevax.
Trước đó, Bộ Y tế đã có hướng dẫn về việc tiêm mũi 3 vắc xin. Trong trường hợp nguồn vắc xin hạn chế, có thể phối hợp tiêm mũi 2 vắc xin do Moderna sản xuất cho người đã tiêm mũi 1 bằng vắc xin do Pfizer hoặc AstraZeneca sản xuất.
Khoảng cách tiêm mũi 2 sau mũi 1 vắc xin do Pfizer sản xuất theo hướng dẫn của nhà sản xuất, khoảng cách sau mũi 1 vắc xin do Astrazeneca sản xuất theo công văn số 7820/BYT-DP ngày 20/9/2021 của Bộ Y tế.