Bộ Y tế thu hồi phiếu tiếp nhận công bố 11 mỹ phẩm gian dối
Tin Y tế - Ngày đăng : 17:24, 23/09/2024

Mới đây, Cục Quản lý Dược, Bộ Y tế vừa có quyết định thu hồi 11 số tiếp nhận phiếu công bố sản phẩm mỹ phẩm của Công ty Cổ phần Dược mỹ phẩm quốc tế LUPACELL.
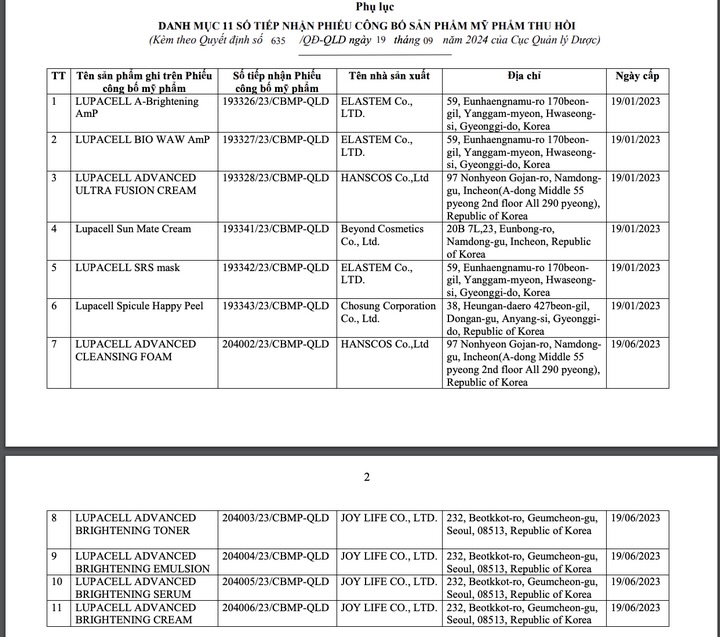
Các sản phẩm mỹ phẩm bị thu hồi phiếu công bố gồm: Lupacell A-Brightening AmP (phiếu công bố số 193326/23/CBMP-QLD 19.1.2023); Lupacell Bio Waw AmP (phiếu công bố số 193327/23/CBMP-QLD 19.1.2023); Lupacell Advanced Ultra Fusion Cream (phiếu công bố số 193328/23/CBMP-QLD 19.1.2023);
Lupacell Sun Mate Cream (phiếu công bố số 193341/23/CBMP-QLD 19.1.2023); Lupacell S.R.S Mask (phiếu công bố 193342/23/CBMP-QLD 19/1/2023); Lupacell Spicule Happy Peel (phiếu công bố số 193343/23/CBMP-QLD 19.1.2023; Lupacell Advanced cleansing Foam (phiếu công bố số 204002/23/CBMP-QLD 19.6.2023)… và các sản phẩm khác.
Theo Cục Quản lý Dược, phiếu công bố của các sản phẩm làm đẹp, chăm sóc tóc do Công ty Cổ phần Dược mỹ phẩm quốc tế LUPACELL chịu trách nhiệm đưa ra thị trường bị thu hồi với lý do kê khai không trung thực các nội dung trong phiếu công bố sản phẩm mỹ phẩm.
Được biết, theo quy định của Bộ Y tế, mỗi sản phẩm mỹ phẩm khi đưa ra lưu thông trên thị trường phải có hồ sơ thông tin sản phẩm (PIF - Product Information File) theo hướng dẫn của ASEAN lưu giữ tại địa chỉ của tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường.
Hồ sơ thông tin sản phẩm mỹ phẩm gồm: Tài liệu hành chính và tóm tắt về sản phẩm; Chất lượng của nguyên liệu; Chất lượng của thành phẩm; An toàn và hiệu quả.
Theo quy định, phần tài liệu hành chính và tóm tắt về sản phẩm của Hồ sơ này phải được xuất trình ngay cho cơ quan kiểm tra, thanh tra khi được yêu cầu; các phần khác nếu chưa đầy đủ thì xuất trình trong vòng 15-60 ngày kể từ ngày kiểm tra theo yêu cầu của cơ quan chức năng.
Số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm là số do cơ quan quản lý nhà nước có thẩm quyền cấp khi tiếp nhận hồ sơ công bố sản phẩm mỹ phẩm. Số này có giá trị chứng nhận sản phẩm mỹ phẩm đã được tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường khai báo với cơ quan quản lý nhà nước có thẩm quyền về việc mỹ phẩm sẽ được lưu thông trên thị trường, không có giá trị chứng nhận sản phẩm đó đảm bảo tính an toàn, hiệu quả, đáp ứng tất cả các yêu cầu của Hiệp định Mỹ phẩm ASEAN và các phụ lục (Annexes) kèm theo.
